再発を繰り返すシビアなRVO症例に対するアイリーアによる治療提案
CRVO/虚血型BRVOに伴う黄斑浮腫は、視力低下・黄斑浮腫悪化のリスクのあるシビアな症例と考えられます

FA(fluorescein angiography):フルオレセイン蛍光眼底造影
* 10DA以上の毛細血管閉塞と定義(VIBRANT試験)。なお、BVOS†では、FAで5乳頭径以上の無灌流領域があれば虚血型とされた。
† BVOS:Branch Retinal Vein Occlusion Study Group
- 1)
- 戸張幾生:網膜静脈閉塞症, メディカル葵出版, 2002, p16.などを参照
- 2)
- 白神史雄(編):専門医のための眼科診療クオリファイ8 網膜血管障害, 中山書店, 2011, p113-116.などを参照
- 3)
- 柳靖雄:あたらしい眼科 2013; 30(2): 155-163. などを参照
- 4)
- バイエル薬品社内資料[日本人を含む第Ⅲ相国際共同試験:VIBRANT試験]承認時評価資料
- 5)
- Shroff D, et al.: Int Ophthalmol. 2008; 28(4): 261-268.
- 6)
- 吉田宗徳:あたらしい眼科 2011; 28(2): 183-190.
- 7)
- The Central Vein Occlusion Study Group: Arch Ophthalmol. 1997; 115(4): 486-491.
多くの先生が、半年以内にBRVOに伴う黄斑浮腫が治癒する患者の割合は50%以下と回答されています
実臨床において、治療開始後6ヵ月以内に治癒する患者(治療の必要がない患者)の割合は?

対象:
本邦の基幹病院に勤務中の網膜専門医41名
方法:
2017年5月28日に日本におけるBRVOの治療実態を明らかにするためのアンケート調査を実施した。スクリーン上に計37問の設問を提示し、アンサーパッドを用いて回答を集計した。
利益相反:
BRVO管理に関する本専門医会議は、バイエル薬品の主催により実施された。バイエル薬品は、本論文のメディカルライティングおよび編集サポートに関する資金提供を行った。著者には、バイエル薬品よりコンサルタント料、講演・講義料、寄付金を受領している者、参天製薬より講演・講義料、寄付金を受領している者が含まれる。
Ogura Y, et al.: Jpn J Ophthalmol. 2019; 63(5): 365-373. より作成
BRVOに伴う黄斑浮腫で再発を繰り返す症例には特徴があります
虚血型/中等度虚血型

毛細血管瘤(MA)を有する症例
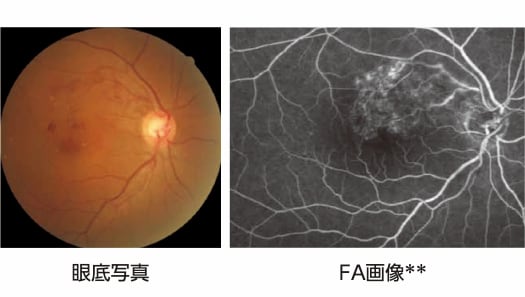
Major BRVO

高齢者***

監修:東京医科大学八王子医療センター眼科 准教授 野間英孝先生
* 光干渉断層計画像
** 蛍光眼底造影画像
*** Noma H, et al.: Ophthalmologica. 2016; 236: 228-234.
OCTA:optical coherence tomography angiography
Nagasato D, et al.: Ophthalmol Retina. 2022
Nagasato D, et al.: Ophthalmol Retina. 2022; 6(7): 567-574.
試験概要
目的
BRVOに伴う黄斑浮腫に対するPRNレジメンを用いた抗VEGF薬治療において、中心窩厚変動が視力および形態学的なアウトカムに及ぼす影響を検討する。
試験デザイン
後ろ向き観察研究
試験対象
2012~2021年の間に複数の施設で抗VEGF薬治療を開始した未治療のBRVOに伴う黄斑浮腫を有する患者309例309眼
投与方法
初期治療として抗VEGF薬1回または3回毎月投与後、OCTにより中心窩に黄斑浮腫または漿液性網膜剥離を認めた場合にPRN投与を行った。
評価項目
最高矯正視力(BCVA)の変化、中心窩厚の変化、中心窩厚変動とBCVAの関係性 など
解析計画
観察期間中の黄斑浮腫再発の程度を評価するため、ベースラインを除く来院時に測定された中心窩厚に基づき、各患者の中心窩厚の標準偏差を算出し、中心窩厚変動と定義した。中心窩厚変動を昇順に4つのグループ(グループ0~3)に均等に分類したうえで、グループ間でのBCVAを比較し、中心窩厚変動とBCVAの関係性を評価した。
利益相反
著者にバイエル薬品より研究費、講演料、謝礼などを受領している者が含まれる。
PRN:pro re nata
BCVA:best-corrected visual acuity
BRVOにおいて中心窩厚変動が大きい症例は視力結果が不良であり、経時的に最高矯正視力が低下する傾向を示しました
中心窩厚変動とBCVAの関係性

中心窩厚変動:ベースラインを除く来院時に測定された中心窩厚に基づき、各患者の中心窩厚の標準偏差を算出し、昇順に4つのグループ(グループ0~3)に均等に分類
Group 0:0-<9.14 ※minimum SD
Group 1:9.14-<34.31
Group 2:34.31-<84.07
Group 3:84.07-<1,117 ※maximum SD
安全性
論文中に副作用・有害事象の発現例に関する記載はありませんでした。
(安全性情報はDIをご参照ください。)
注意:試験実施国(オーストラリア)および本邦において、ベバシズマブの網膜静脈閉塞症への適応は未承認である。
Spooner K, et al.: Clin Exp Ophthalmol. 2020
(海外データ)
Spooner K, et al.: Clin Exp Ophthalmol. 2020; 48: 53-60.
試験概要
目的
RVOに伴う持続性の黄斑浮腫の治療において、前治療薬(ベバシズマブまたはラニビズマブ)からアイリーアへ切替えた際の効果を検討する。
試験デザイン
非無作為化、オープンラベル、前向き、単群切替試験
試験対象
RVOに伴う黄斑浮腫を有する患者18例18眼
(BRVO:14例、CRVO:4例)
[主な選択基準]
- 前治療薬の最終投与4週後にRVOに伴う持続性の黄斑浮腫を認める(中心網膜厚[CMT]>320μm)
- スクリーニング時のETDRS視力表による最高矯正視力(BCVA)文字数が73~34文字(スネレン視力で6/12~6/60)
投与方法
前治療薬(ベバシズマブまたはラニビズマブ)による治療※の後に、アイリーア2.0mgへの切替を実施した。切替後8週までは、4週ごとに 3回投与し(ベースライン、切替後4週、切替後8週)、以降は48週目まで8週ごとに投与した。
評価項目
- 主な評価項目:切替後48週時のBCVA文字数のベースラインからの変化量、CMTのベースラインからの変化量
- その他の評価項目:切替後4週ごとのBCVA文字数およびCMTのベースラインからの変化量 など
解析計画
BCVA文字数およびCMTのベースラインからの変化量について、対応のあるt検定を用いて解析した。
利益相反
本試験はBayer Corporation Global の資金提供により実施された。著者にBayerのコンサルタントを務めている者およびBayer Australiaより旅費を受領している者が含まれる。
※前治療薬(ベバシズマブまたはラニビズマブ)の平均投与回数:40.0±17.8回、平均観察期間:75.6±43.3ヵ月
CMT:central macular thickness
ETDRS:early treatment diabetic retinopathy study
BRVOに伴う黄斑浮腫患者においてアイリーア投与開始後48週時、最高矯正視力文字数のベースラインからの変化量は+21.1文字であり、有意な改善を示しました
最高矯正視力文字数のベースラインからの変化量の推移

Spooner K, et al.: Clin Exp Ophthalmol. 2020; 48: 53-60. より一部改変
BRVOに伴う黄斑浮腫患者においてアイリーア投与開始後48週時、中心網膜厚のベースラインからの変化量は-87.6μmであり、有意な減少を示しました
中心網膜厚のベースラインからの変化量の推移

Spooner K, et al.: Clin Exp Ophthalmol. 2020; 48: 53-60. より一部改変
安全性
- 本試験において、虚血性心筋梗塞またはその他の血栓塞栓症の発現は認められませんでした。
- 試験期間中に1例がパーキンソン病と診断されましたが、抗VEGF薬との関連は否定されました。
- 試験期間中に眼内炎、血管新生緑内障、網膜虚血の明らかな進行の発現は認められませんでした。
その他の有害事象については論文に記載されていませんでした。
Casselholm de Salles M, et al.: Retina. 2019
(海外データ)
Casselholm de Salles M, et al.: Retina. 2019; 39: 1370-1376.
試験概要
目的
CRVOに伴う黄斑浮腫の治療において、アイリーアおよびラニビズマブの投与回数を前向きに比較検討する。観察期間18ヵ月、無作為化、前向き、二重遮蔽試験
試験対象
CRVO(罹病期間12ヵ月以下)に伴う黄斑浮腫※を有する18歳超の未治療患者45例
投与方法
- アイリーア群(22例)またはラニビズマブ群(23例)に1:1の割合で無作為に割り付け、Treat & Extend(T&E)投与レジメンで治療を行い、18ヵ月間観察する。
- 導入期には、アイリーア2.0mg、ラニビズマブ0.5mgをそれぞれ4週ごとに3回投与し、以降は投与間隔を2週ずつ、最長12週まで延長する。
- 黄斑浮腫(OCTにより網膜内液または網膜下液を検出)が認められた場合は、投与間隔を2週ずつ、最短4週まで短縮する。
評価項目
- 主要評価項目:18ヵ月間の投与回数
- 副次的評価項目:15文字以上の視力改善がみられた患者の割合、BCVA変化量、CRT変化量、試験終了時の投与間隔
解析計画
- 投与回数および投与間隔の解析対象は、導入期投与を完了した全患者(ITT)および全観察期間を完了した患者(PP)とする。
- ITTの欠測値は、LOCF法を用いて補完する。投与回数は、最後に観察した投与間隔で残りの期間を投与したと仮定し算出する。
※黄斑浮腫の定義:網膜嚢胞あり、OCTでCRTが300μmより高い、BCVAがETDRSでは73~23文字、Snellen等価視力では20/40~20/320
ITT:intent-to-treat
PP:per protocol
LOCF:last observation carried forward
<主要評価項目>
CRVOに伴う黄斑浮腫患者において18ヵ月間の平均投与回数はアイリーア群で10.9回であり、ラニビズマブ群の14.4回に比べて有意に少ないことが示されました
投与回数(LOCF、ITT)

* p<0.05, independent Student’s t検定
<副次的評価項目>
18ヵ月目におけるアイリーアの平均投与間隔は10.0週であり、ラニビズマブ群に比べて有意に長いことが示されました
18ヵ月目における投与間隔の内訳(LOCF、ITT)
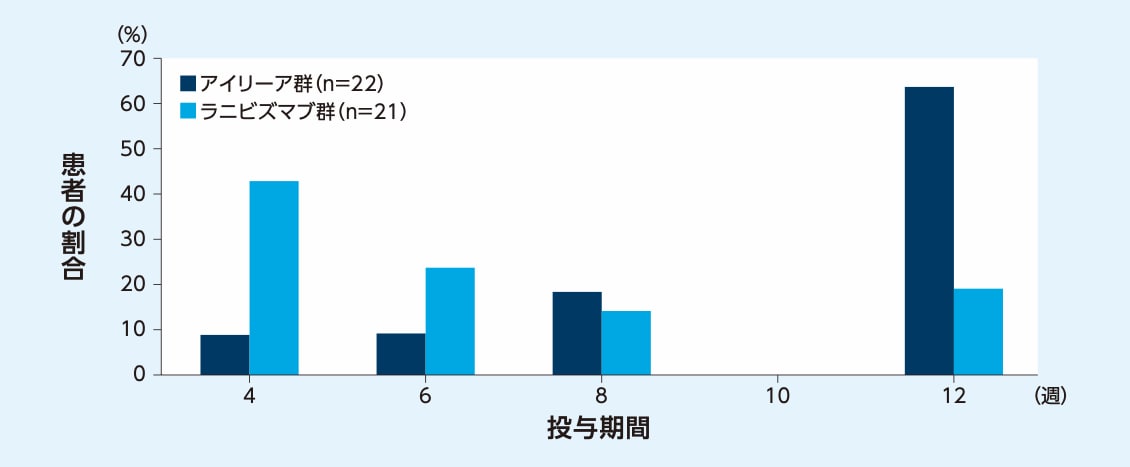
18ヵ月目における投与間隔(LOCF、ITT)

* independent Student’s t検定
安全性
- 重篤な有害事象として、アイリーア群では心筋梗塞、大動脈瘤破裂が各1例、ラニビズマブ群では心筋梗塞が1例で発現しました。
- そのうち、死亡に至った重篤な有害事象はアイリーア群の心筋梗塞、大動脈瘤破裂の2例でした。
- 試験期間中に眼内炎、網膜裂孔、網膜剥離の発現は認められませんでした。
- 試験終了時までに7例が脱落しました。脱落理由の内訳はノンレスポンダーが2例(いずれもラニビズマブ群)、心筋梗塞が2例(アイリーア群、ラニビズマブ群各1例)、大動脈瘤破裂(アイリーア群)、ETDRS視力表によるBCVAが0文字、患者希望による中止(いずれもラニビズマブ群)が各1例でした。
CRVO/BRVOともに眼内VEGF濃度が上昇し、黄斑浮腫などの病態に関与していると考えられています
CRVOに伴う黄斑浮腫を有する患者における
VEGF濃度
- 眼内VEGF濃度が上昇している1, 2)。
- VEGF濃度は黄斑浮腫の程度(網膜厚)と相関する2)。
- VEGF濃度は非虚血型よりも虚血型で高い1, 2)。

【対象・方法】
2003~2007年に東京女子医科大学または広島大学病院において、硝子体切除術を受けたCRVOに伴う黄斑浮腫を有する患者27例、および特発性網膜前膜または黄斑円孔を有する患者16例の、硝子体内VEGF濃度を比較検討した。
- 1)
- Noma H, et al.: Ophthalmology. 2009; 116: 87-93.
利益相反:本論文の著者にBayerより謝礼を受領した者が含まれる。
- 2)
- Noma H, et al.: Invest Ophthalmol Vis Sci. 2015; 56: 1122-1128.
利益相反:本論文の著者にBayerより謝礼および研究費を受領した者が含まれる。
BRVOに伴う黄斑浮腫を有する患者における
VEGF濃度
- 眼内VEGF濃度が上昇している3, 4)。
- VEGF濃度は、罹病期間・黄斑浮腫の程度(網膜厚)・無灌流領域面積と相関する3, 4)。

【対象・方法】
NTT東日本東北病院における倫理委員会の承認のもと、2004~2006年に硝子体切除術を受けたBRVOに伴う黄斑浮腫を有する患者60例、および特発性網膜前膜または特発性黄斑円孔を有する患者12例の、硝子体内VEGF濃度を比較検討した。
- 3)
- Shimura M, et al.: Acta Ophthalmol. 2008; 86: 377-384.
利益相反:本論文の著者にBayerより謝礼および研究費を受領した者が含まれる。
- 4)
- Noma H, et al.: Invest Ophthalmol Vis Sci. 2014; 55: 3878-3885.
利益相反:本論文の著者にBayerより謝礼および研究費を受領した者が含まれる。
VEGF-A165とVEGF受容体1および受容体2との結合阻害作用を示すIC50は、アフリベルセプトではそれぞれ16pM、26pMでした
抗VEGF薬のVEGF-VEGF受容体結合の阻害作用(IC50, in vitro)

IC50(50%阻害濃度):阻害の強さを示す値。数値が小さいほど低濃度でリガンドと受容体との結合を50%阻害したことを示す。
NB:no detectable binding
【試験方法】
VEGF受容体1またはVEGF受容体2を発現させたHEK293細胞を用いて、20pMヒトVEGF(hVEGF)-Aあるいは40pMヒトPlGF(hPlGF)と各種VEGF受容体の結合に対するアフリベルセプトおよびラニビズマブの50%阻害濃度(IC50)を算出した。
Papadopoulos N, et al.: Angiogenesis. 2012; 15(2): 171-185. より一部改変
利益相反:本論文の著者全員がRegeneron社の社員である。
まとめ
アイリーアはCRVOや虚血型BRVOのようなシビアな症例において、効果が期待できるVEGFファミリー阻害薬です
RVOにはCRVOや虚血型BRVOのような視力低下・黄斑浮腫悪化のリスクのあるシビアな症例が存在します1〜7)。BRVOにおいて中心窩厚変動が大きい症例は視力結果が不良であり、経時的に最高矯正視力が低下する傾向を示しました8)。
Spooner K, et al.: Clin Exp Ophthalmol. 20209)(海外データ)
BRVOに伴う黄斑浮腫患者においてアイリーア投与開始後48週時、主な評価項目である最高矯正視力文字数のベースラインからの変化量は+21.1文字であり、有意な改善を示しました。また主な評価項目である中心網膜厚のベースラインからの変化量は-87.6μmであり、有意な減少を示しました。
本試験において、虚血性心筋梗塞またはその他の血栓塞栓症の発現は認められませんでした。試験期間中に1例がパーキンソン病と診断されましたが、抗VEGF薬との関連は否定されました。その他の有害事象については、論文に記載されていませんでした。
Casselholm de Salles M, et al.: Retina. 201910)(海外データ)
CRVOに伴う黄斑浮腫患者において18ヵ月間の平均投与回数はアイリーア群で10.9回であり、ラニビズマブ群の14.4回に比べて有意に少ないことが示されました。
重篤な有害事象として、アイリーア群では心筋梗塞、大動脈瘤破裂が各1例、ラニビズマブ群では心筋梗塞が1例で発現しました。そのうち、死亡に至った重篤な有害事象はアイリーア群の心筋梗塞、大動脈瘤破裂の2例でした。
VEGF-A165とVEGF受容体1および受容体2との結合阻害作用を示すIC50は、アフリベルセプトではそれぞれ16pM、26pMでした11)。
- 1)
- 戸張幾生:網膜静脈閉塞症, メディカル葵出版, 2002, p16.などを参照
- 2)
- 白神史雄(編):専門医のための眼科診療クオリファイ8 網膜血管障害, 中山書店, 2011, p113-116.などを参照
- 3)
- 柳靖雄:あたらしい眼科 2013; 30(2): 155-163.などを参照
- 4)
- バイエル薬品社内資料[日本人を含む第Ⅲ相国際共同試験:VIBRANT試験]承認時評価資料
- 5)
- Shroff D, et al.: Int Ophthalmol. 2008; 28(4): 261-268.
- 6)
- 吉田宗徳:あたらしい眼科 2011; 28(2): 183-190.
- 7)
- The Central Vein Occlusion Study Group.: Arch Ophthalmol. 1997; 115(4): 486-491.
- 8)
- Nagasato D, et al.: Ophthalmol Retina. 2022; 6(7): 567-574.
- 9)
- Spooner K, et al.: Clin Exp Ophthalmol. 2020; 48: 53-60.
- 10)
- Casselholm de Salles M, et al.: Retina. 2019; 39: 1370-1376.
- 11)
- Papadopoulos N, et al.: Angiogenesis. 2012; 15(2): 171-185.



