日本人を含む第Ⅲb相国際共同試験:FIREFLEYE NEXT試験1-3)
(長期安全性および視機能の評価)[中間解析、2歳時]
1)バイエル薬品社内資料[日本人を含む第Ⅲb相国際共同試験:FIREFLEYE NEXT試験]承認時評価資料
2)Stahl A, et al.: JAMA Netw Open. 2024; 7: e248383.
3)FIREFLEYE NEXT試験 社内資料
アイリーア(2mg)の承認された効能又は効果(抜粋):未熟児網膜症*
アイリーア(2mg)の承認された用法及び用量(抜粋):
〈未熟児網膜症〉
アフリベルセプト(遺伝子組換え)として1回、0.4mg(0.01mL)を硝子体内投与する。なお、必要な場合は再投与できるが、1ヵ月以上の間隔をあけること。
*
本適応症は「アイリーア®硝子体内注射液40mg/mL」の効能又は効果として承認されています。「アイリーア®硝子体内注射用キット40mg/mL」の効能又は効果としては承認されていません
本ページでは「アイリーア(2mg)」を「アイリーア」と記載しています。
試験概要

【実施地域】FIREFLEYE NEXT試験:アジア太平洋地域(日本含む)、欧州、ラテンアメリカ、中東の24ヵ国、55施設
目的
FIREFLEYE試験で試験治療を受けたROP患者を対象に、アイリーアの長期安全性、視機能、および発達全般について検討する
対象
ROP患者100例(うち日本人:13例)
[主な選択基準]
- FIREFLEYE試験で試験治療を受けた
- 暦年齢が13ヵ月未満 など
[除外基準]
本試験への参加または試験手順の実施を妨げる医学的状態を有する
デザイン
非無作為化非遮蔽網膜光凝固術対照比較試験
投与方法
FIREFLEYE NEXT試験では試験治療を行わなかった。なお、ROPに対する治療が必要となった場合、治験担当医師の判断により各国の標準治療に従って試験治療以外の治療を実施できた。
![FIREFLEYE NEXT試験[中間解析、2歳時]:投与方法の図](/sites/g/files/vrxlpx7866/files/2024-09/safety_rop_firefleye_next2_img01.png)
a)
スクリーニング/追跡調査開始時来院は、FIREFLEYE試験の24週目の来院日または最終追跡調査来院日のうちいずれか遅い方の日と同日、もしくはこの日から患者の暦年齢が13ヵ月になるまでの期間のいずれかとした。
b)
本試験に組入れられた患者の50%以上で、1歳時データが得られた時点をデータカットオフ日とした。
c)
1歳の誕生日の前後1ヵ月に検査を実施した。
d)
2歳の誕生日の前1ヵ月から後3ヵ月に検査を実施した。
e)
中間解析時(2歳時)において評価時点未達
主な有効性評価項目
主要評価項目:
5歳時の両眼視での最高矯正視力(Snellen換算スコア)
副次評価項目:
- 1、3および5歳時に不良な形態学的転帰(網膜剥離、黄斑牽引、黄斑皺襞または水晶体後部組織)を認めた患者の割合※1
- 1歳時に活動性のROPがなく、かつ不良な形態学的転帰もない患者の割合※2
- 3および5歳時の各眼における等価球面屈折度※3 など
事前に規定したその他の評価項目:
- 5歳時までの視機能および屈折ならびに形態学的転帰の評価※3,4
- 5歳時までの斜視検査結果の解析※3,5
- 5歳時までの倒像検眼鏡検査に基づき血管の発達の完了を認めた患者の割合※3,6 など
主な安全性評価項目
有害事象、重篤な有害事象、投与中止に至った有害事象、死亡、理学的検査、発達検査※7 など
解析計画
探索的な解析
主要評価項目(FAS)
副次評価項目(FAS)
事前に規定したその他の評価項目(FAS)
※1
1および2歳時の結果を掲載
※2
2歳時にROPがない患者の割合を掲載
※3
2歳時の結果を掲載
※4
視機能を掲載
※5
眼球運動
※6
眼の割合を掲載
※7
BSID-Ⅲ、VABS-Ⅱ
FAS(full analysis set):最大の解析対象集団、BSID-Ⅲ(Bayley Scales of Infant and Toddler Development, Third Edition): BayleyⅢ乳幼児発達検査、VABS-Ⅱ(Vineland Adaptive Behavior Scales, Second Edition): VinelandⅡ適応行動尺度
試験対象例数と各群の患者の内訳
![FIREFLEYE NEXT試験[中間解析、2歳時]:試験対象例数と各群の患者の内訳の図](/sites/g/files/vrxlpx7866/files/2024-09/safety_rop_firefleye_next2_img02.png)
FIREFLEYE NEXT試験の患者背景および特性(FAS)

a)
標準的な人口統計学的パラメータの一部として収集され、治験担当医師が医療記録および親から提供された情報を考慮し、固定カテゴリーを用いて分類した。
b)
黒人またはアフリカ系アメリカ人および白人
c)
ROPの病期(zoneおよびstage)がより進行している眼に基づき分類した。
より進行している眼の選択基準:AP-ROPまたはzoneがより低い眼とし、同じ場合は、stageがより高い眼を選択した。
[zone、AP-ROP、stageについて]
zoneⅠ:視神経乳頭の中心から中心窩の中心までの推定距離の2倍を半径とした最も後極側の円の領域
zoneⅡ:zoneⅠの外側で視神経乳頭の直径の2倍に及ぶ環状の領域
zoneⅢ:zoneⅡの外側の三日月状の領域
AP-ROP:zoneⅠまたはzoneⅡで急速に進行するROP
stage1:網膜に有血管領域と無血管領域の境界線がある
stage2:隆起がある
stage3:隆起に網膜外線維血管増殖がある
stage4A:中心窩を含まない網膜部分剥離
stage4B:中心窩を含む網膜部分剥離
stage5:網膜全剥離
+:後極部の網膜血管の静脈拡張および動脈蛇行
AP-ROP(aggressive-posterior ROP)
FIREFLEYE試験の患者背景および特性(FASa))

a)
SAFと同数である。
b)
FIREFLEYE試験での試験治療開始時の最低体重は800gであった。
SAF(safety analysis set):安全性解析対象集団
5歳時の両眼視での最高矯正視力(Snellen換算スコア)(FAS):主要評価項目
中間解析時(2歳時)においてデータは得られていない。
2歳時までに不良な形態学的転帰を認めた患者の割合は、アイリーア投与群で6.1%、レーザー治療群で5.9%でした
1および2歳時に不良な形態学的転帰(網膜剥離、黄斑牽引、黄斑皺襞または水晶体後部組織)を認めた患者の割合(FAS):副次評価項目

例数(%)または眼数(%)
FIREFLEYE試験および/またはFIREFLEYE NEXT試験で報告されたすべての不良な形態学的転帰を含む。
片眼に対し2つ以上の形態学的転帰を認める場合がある。
1歳時または2歳時来院前に試験を中止した患者も解析に含め、不良な形態学的転帰を認めた場合は、当該事象を解析に含めた。
2歳時にROPがない患者の割合は、アイリーア投与群で96.8%、レーザー治療群で93.8%でした
2歳時にROPがない患者の割合(FAS):副次評価項目

2歳時の等価球面屈折度数(平均値)は、アイリーア投与群で-0.6ディオプター、レーザー治療群で-1.9ディオプターでした
2歳時の各眼における等価球面屈折度数(FAS):副次評価項目

調節麻痺下での屈折検査
等価球面屈折度数:球面屈折値+1/2円柱屈折値
強度近視:-5ディオプター(破線)以下
重度の強度近視:-8ディオプター(点線)以下
2歳時に血管の発達の完了を認めた眼の割合は、アイリーア投与群で80.2%でした
2歳時までの倒像検眼鏡検査に基づき血管の発達の完了を認めた眼の割合(FAS):事前に規定したその他の評価項目

眼数(%)
2歳時に5cmの玩具の固視および追視ができた眼の割合は、アイリーア投与群で96.7%、レーザー治療群で98.4%でした
2歳時までの視機能および形態学的転帰の評価/斜視検査結果の解析(FAS):事前に規定したその他の評価項目

眼数(%)
FIREFLEYE NEXT試験(2歳時まで)における安全性(SAF)
有害事象発現率
アイリーア投与群で66例中53例(80.3%)、レーザー治療群で34例中27例(79.4%)に認められました
主な有害事象
アイリーア投与群:上咽頭炎12例(18.2%)、上気道感染11例(16.7%)、発熱、気管支炎、近視、乱視、斜視が各9例(13.6%)
レーザー治療群:発熱、気管支炎が各6例(17.6%)、近視5例(14.7%)、COVID-19、乱視が各4例(11.8%)
試験薬に関連する重篤な有害事象
アイリーア投与群:網膜剥離1例(1.5%)
レーザー治療群:本試験においては認められませんでした
試験薬に関連する投与中止に至った有害事象、試験薬に関連する死亡
本試験においては認められませんでした
MedDRA ver.25.0
出生日+2年までに発現した事象を示した(集計結果にはFIREFLEYE試験において発現した有害事象を含めた)。
有害事象(2歳時まで)(SAF)

発現例数(発現割合%)
MedDRA ver.25.0
試験眼とはFIREFLEYE試験で試験治療を受けた眼のことを示す。
FIREFLEYE NEXT試験への参加同意時にFIREFLEYE試験から継続的に発現していた重篤な有害事象を含む。
a)
上咽頭炎はいずれも非重篤であり、呼吸器感染症に典型的な他の呼吸器事象に関連しており、試験薬の投与との関連なしと判断された。
b)
片眼の視神経萎縮は網膜剥離に続発し、1歳時点で重篤な有害事象として報告され、FIREFLEYE試験の試験治療との関連なしと判断された。当該患者は、1歳時点で対光反応が正常であったが、5cmの玩具の固視および追視ができなかった。2歳時点では5cmの玩具の固視および追視ができた。対側眼では5cmの玩具の固視および追視ができ、対光反応も正常であった。アイリーア投与群の1例では、21ヵ月時点で両眼において脳室内出血および水頭症に続発する視神経萎縮が認められた(非重篤、FIREFLEYE試験の試験治療との関連なし)。当該患者は両眼において5cmの玩具の固視および追視ができ、対光反応も正常であった。アイリーア投与群ではその他に、FIREFLEYE試験の試験治療開始から24週目に両眼で視神経萎縮が認められ、2歳時点では消失したと報告された患者がいたものの、本報告は検討が必要である。
c)
FIREFLEYE試験において、1例の両眼に軽度と中等度の網膜芽細胞腫が認められた。両眼ともにFIREFLEYE NEXT試験の追跡調査開始時には未回復であった。2歳時点で左眼は未回復と報告され、右眼は不明と報告された。両事象ともに試験薬との関連なしと判断された。
全身性の重篤な有害事象(2歳時まで)(SAF)

発現例数(発現割合%)
MedDRA ver.25.0
理学的検査(2歳時)(SAF)

平均値(標準偏差)
発達検査①(2歳時)(SAF)
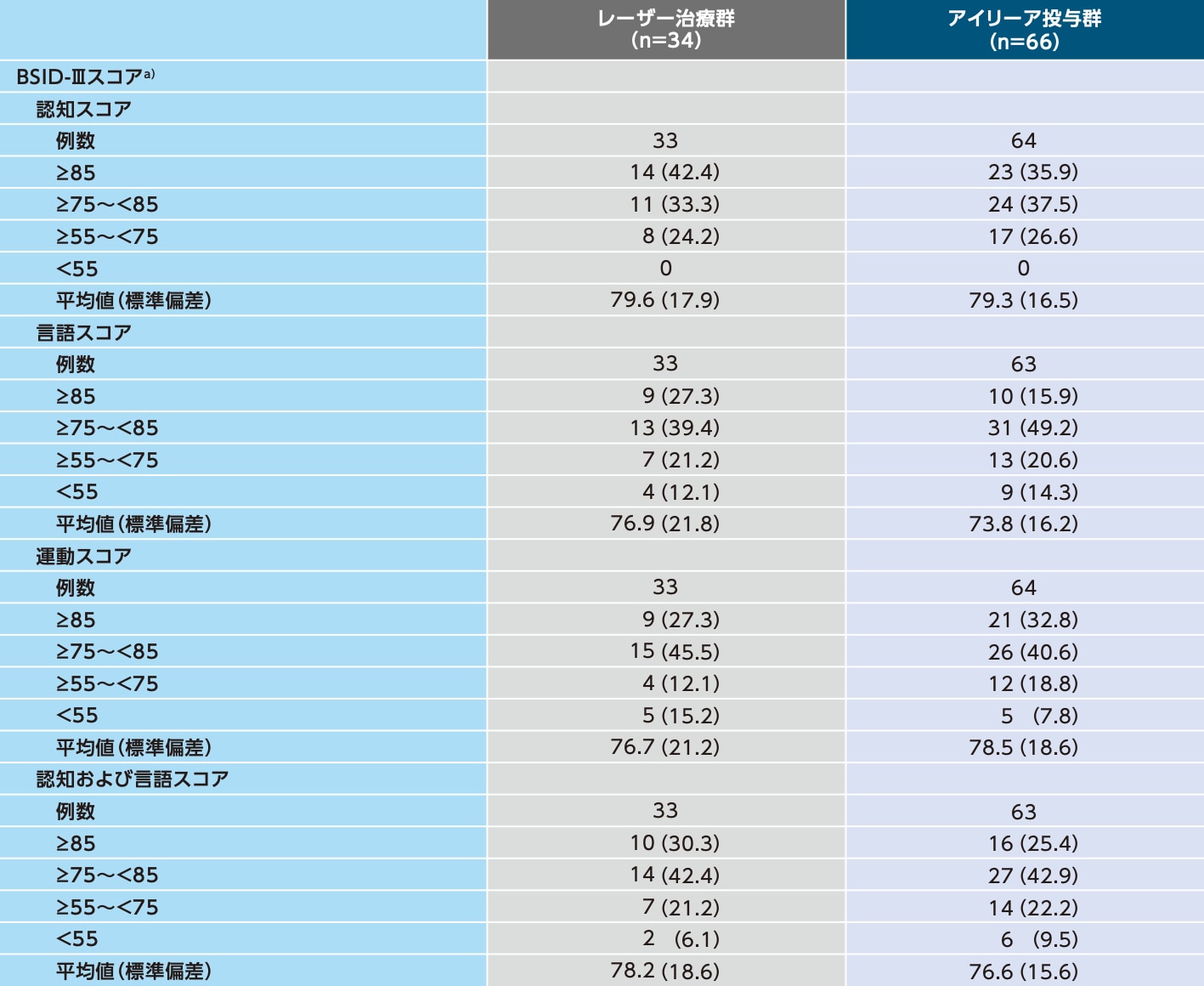
例数(%)
a)スコアが高いほど機能が高いことを示す。
発達検査②(2歳時)(SAF)

例数(%)
Limitations:
本結果には、中間解析の探索的性質と統計解析の記述的性質が含まれることによる制限がある。 FIREFLEYE試験では、ROPの重症度のみにより層別化され無作為化されたため、各群の異質性は排除できない可能性がある。重度のROP患者は少ないためFIREFLEYE試験のサンプルサイズも比較的小さい。ROP患者に対するレーザー治療の有効性に関する公開データに基づき、FIREFLEYE試験の患者は試験治療開始時にアイリーア0.4mgを硝子体内注射する群とレーザー治療を行う群に2:1に無作為に割り付けられたため、本試験のレーザー治療群はアイリーア投与群よりも例数が少ない。血管の発達の完了の評価は、超広角眼底検査やフルオレセイン蛍光眼底造影でなく、倒像検眼鏡検査によって行われており、これも制限となる可能性がある。試験に参加した24ヵ国それぞれにバリデーションされたデータがなかったため、BSID-Ⅲの結果の解析には米国で使用される標準化データが用いられた。レーザー治療を行うことで網膜にレーザー瘢痕が見えることから、他のROP試験と同様に治療群の割り付けは非遮蔽で実施された。



